Aprobación regulatoria: qué implica realmente
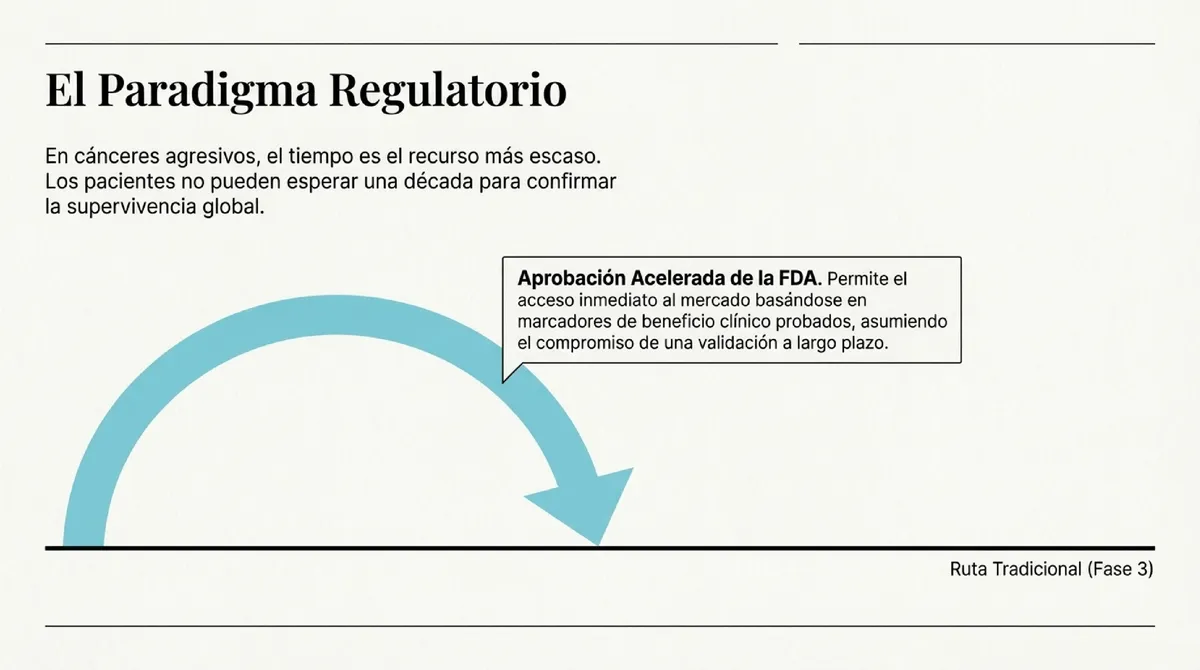
Escenario: Un laboratorio biotecnológico presenta datos prometedores en un tipo de cáncer agresivo con pocas opciones de tratamiento. Los pacientes no pueden esperar los 5 o 10 años que suele tardar un ensayo clínico fase 3 convencional para confirmar la supervivencia global. ¿Cómo decide la FDA permitir que el fármaco llegue al mercado hoy sin tener todavía la certeza absoluta de su beneficio clínico a largo plazo?
Key Points: El marco legal de Zepzelca
- Zepzelca entró al mercado bajo el programa de Aprobación Acelerada (Accelerated Approval) de la FDA.
- Esta vía se reserva para enfermedades graves que tienen una necesidad médica no cubierta.
- La aprobación no se basa en "curar", sino en indicadores indirectos como la tasa de respuesta objetiva (ORR).
Accelerated Approval (Aprobación Acelerada): Es una regulación que permite la aprobación de fármacos para condiciones graves basándose en un "endpoint" (punto final) subrogado que es razonablemente probable que prediga un beneficio clínico.
En el caso de Zepzelca, la FDA aceptó que si el tumor se reduce (ORR) y esa reducción dura cierto tiempo (DoR), es probable que el paciente viva más, aunque no se haya demostrado formalmente todavía.
Explicación guiada: De la molécula al negocio
La aprobación acelerada es un "contrato" entre la farmacéutica y el regulador. La FDA otorga el permiso de comercialización anticipado para que los pacientes se beneficien, pero a cambio exige estudios confirmatorios. Si estos estudios fallan en verificar el beneficio clínico (como la supervivencia global), la FDA tiene la potestad de retirar el fármaco del mercado.
Para el perfil de negocio, esto significa que Zepzelca tiene una aprobación condicional. El flujo de ingresos del fármaco depende de que los ensayos posteriores ratifiquen lo observado en el estudio de fase 2.
El "Préstamo de Confianza" Regulatorio
Imagina que la FDA le da una "tarjeta de crédito" a la farmacéutica. El fármaco se vende hoy basándose en el Overall Response Rate (ORR), pero la deuda se debe pagar mañana demostrando Clinical Benefit (beneficio clínico real como vivir más o mejor). Si no se paga la deuda con datos sólidos, se cancela el crédito (la aprobación).
Implicaciones Clínicas y de Mercado
| Concepto | Qué significa | Implicación de Negocio |
|---|---|---|
| Endpoint Subrogado | Usar ORR (reducción del tumor) en lugar de supervivencia. | Llegada al mercado varios años antes de lo previsto. |
| Contingencia | La aprobación depende de ensayos confirmatorios. | Existe un riesgo de retiro del mercado si los datos fallan. |
Errores comunes de interpretación:
- Confundir aprobación acelerada con aprobación total: La acelerada requiere validación posterior; la total ya ha demostrado el beneficio clínico directo.
- Asumir que ORR es igual a supervivencia: Que un tumor se reduzca (o desaparezca visualmente en un escáner) no siempre garantiza que el paciente vivirá más tiempo.
Resumen de la Lección
- Zepzelca es un agente alquilante que obtuvo luz verde mediante una vía regulatoria especial.
- Su aprobación se basa en la Tasa de Respuesta (35%) observada en el estudio B-005.
- El estatus regulatorio actual impone la necesidad de realizar ensayos Fase 3 adicionales.